宿主腸道防御有害微生物侵襲的前線(xiàn):粘液素、抗菌肽和微生物區(qū)系
作者:Vanessa Lievin-Le Moal和Alain L. Servin 翻譯:楊江濤
清遠(yuǎn)容大生物工程有限公司市場(chǎng)技術(shù)部
1、前言
腸道黏膜表面是身體接觸外部環(huán)境最大的表面(200-300m2),這是一個(gè)綜合了胃腸上皮細(xì)胞、免疫細(xì)胞和寄生微生物區(qū)系的復(fù)雜生態(tài)系統(tǒng),腸道粘膜受到各種病原微生物的危脅,這些潛在的有害腸道微生物可以搶奪宿主的細(xì)胞分子和信號(hào)傳導(dǎo)途徑導(dǎo)致發(fā)病。感染過(guò)程中的第一步,一些腸道細(xì)菌病原粘附在腸道細(xì)胞的刷狀緣,它們能夠利用細(xì)胞的信號(hào)途徑,此外,一些腸道病原微生物能夠發(fā)展出專(zhuān)門(mén)的系統(tǒng),在粘附完成以后,這些系統(tǒng)產(chǎn)生毒力因子。在正常的宿主細(xì)胞功能被擾亂以后,這些系統(tǒng)能使病原通過(guò)上皮屏障。在細(xì)胞被滲透過(guò)程中,宿主細(xì)胞骨架通常是被腸道病原微生物攻擊的靶點(diǎn),這樣作的目點(diǎn)包括獲得進(jìn)入細(xì)胞的入口、移動(dòng)到細(xì)胞中和細(xì)胞之間、為了創(chuàng)造一個(gè)專(zhuān)門(mén)的可以提高病原生存機(jī)會(huì)、形成和改造空泡。
腸道上皮細(xì)胞形成物理的和化學(xué)的屏障,保護(hù)宿主不受來(lái)自潛在的腸道有害微生物的攻擊(見(jiàn)圖1)。腸道表面是由一種簡(jiǎn)單的柱狀上皮細(xì)胞排列形成,柱狀上皮細(xì)胞折疊形成大量的深入到連接組織中的內(nèi)陷或隱窩。腸細(xì)胞組織的上皮提一個(gè)保護(hù)宿主對(duì)抗微生物侵?jǐn)_的物理屏障。腸上皮是一類(lèi)可以更新的組織,因?yàn)槟c細(xì)胞可以不斷地由腸隱窩中的一種多功能干細(xì)胞分化產(chǎn)生,而且這些細(xì)胞提供一種高轉(zhuǎn)化率的新前體細(xì)胞。在腸絨毛中,形成上皮的分化的上皮細(xì)胞分成兩類(lèi)不同組成部分。上皮屏障包括 4種上皮細(xì)胞系:腸上皮細(xì)胞、內(nèi)分泌細(xì)胞、杯狀細(xì)胞和潘氏細(xì)胞,這 4 種細(xì)胞在腸絨毛中存在。此外,M細(xì)胞存在于濾泡相關(guān)上皮中。上皮細(xì)胞層的完整是由緊密連接(TJs) 、粘合連接(AJs)和細(xì)胞橋粒組成的細(xì)胞間的連接體來(lái)維持的,然而在縫隙連接允許細(xì)胞間信號(hào)傳遞。緊密連接(TJs)位于連接復(fù)合體的最頂端,形成細(xì)胞單體之間一個(gè)半透性擴(kuò)散屏障,這個(gè)屏障可以被調(diào)控和作為滲透性屏障。TJs中含有 40 種不同的蛋白,例如膜相關(guān)鳥(niǎo)苷酸激酶蛋白家族中的ZO-1、ZO-2 和ZO-3蛋白、Occludin蛋白、Claulin蛋白、7H6 和幾種未確認(rèn)的磷蛋白。有趣的是,TJs的生源學(xué)研究顯示,TJs部分上可能被幾種經(jīng)典的信號(hào)傳導(dǎo)途經(jīng)調(diào)控,例如異三聚體G蛋白、G2+蛋白激酶C和作為信號(hào)分子中轉(zhuǎn)平臺(tái)的船樣膜微區(qū)。TJs的下部是粘合連接(AJs),包括一種鈣粘蛋白/連接素復(fù)合體及其相關(guān)蛋白、膜和PDZ蛋白。在TJs和AJs中,上皮細(xì)胞連接復(fù)合休形成過(guò)程中,他們中的特異性成分可以在動(dòng)力調(diào)控作用下產(chǎn)生交互作用。重要的是,TJs和AJs在維持細(xì)胞分化中起到關(guān)鍵作用。甚至,最近的證據(jù)顯示無(wú)論TJs是否存在,細(xì)胞分化運(yùn)動(dòng)能形成針對(duì)擴(kuò)散的膜內(nèi)屏障,限制細(xì)胞膜頂部和底部成分的混合。令人感興趣的是,許多致病性腸細(xì)菌以TJ區(qū)域作為靶位和攻擊對(duì)象從而改變腸道滲透性,造成發(fā)病。現(xiàn)在經(jīng)確認(rèn),一些腸道病原體使用覆蓋組織粘膜相關(guān)淋巴系統(tǒng)的M細(xì)胞作為感染途徑,它們通過(guò)這些細(xì)胞以后,細(xì)菌面臨噬菌細(xì)胞、位于濾泡頂部的特異性巨噬細(xì)胞。
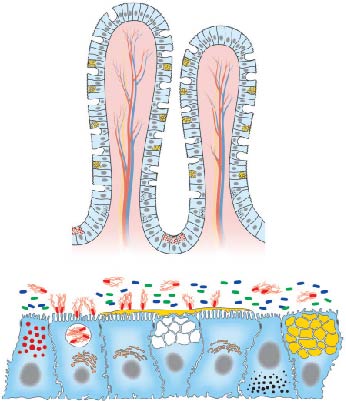
圖 1:腸道中腸上皮細(xì)胞排列結(jié)構(gòu)
(A)隱窩絨毛細(xì)胞組織。細(xì)胞更新是從多功能腸干細(xì)胞中獲得,小腸中是從隱窩基部的上端,結(jié)腸是在隱窩基部。上皮遷移到隱窩上端,這里他們呈顯出差異,獲得吸收和分泌的特異性功能。當(dāng)他們遷移時(shí), 三種類(lèi)型的區(qū)別表現(xiàn)出來(lái):主要的腸上皮細(xì)胞、分泌粘液杯狀細(xì)胞和分泌肽激素的內(nèi)分泌細(xì)胞。相對(duì)的,潘氏細(xì)胞遷移到隱窩基部。
(B)分化的上皮細(xì)胞匯集一起,形成一個(gè)在內(nèi)部與外部之間具有滲透性的上皮。
該屏障的功能由連接區(qū)域決定的,包括界面清楚的縫隙連接、細(xì)胞橋粒、粘合連接和緊密連接。腸上皮出現(xiàn) 4 種分化的上皮細(xì)胞系:腸上皮細(xì)胞表達(dá)在頂端,排列密集,刷狀緣界面整齊,包括導(dǎo)向性蛋白的支持特別功能的膜上的組織分明微絨毛;粘液分泌杯狀細(xì)胞(有黃色大顆粒的細(xì)胞)產(chǎn)生結(jié)合細(xì)胞膜的粘液素和包含成熟的貯存顆粒,貯存顆粒中包裹著分泌的粘液素;內(nèi)分泌細(xì)胞(有黑色小顆粒的細(xì)胞)包含形狀小、導(dǎo)向性分泌顆粒,盡管 1 個(gè)小顆粒可以貯存多種肽激素,在顆粒中貯存不同的肽激素;潘氏細(xì)胞(有紅色小顆粒的細(xì)胞)包含在頂端的導(dǎo)向性顆粒,在這些顆粒中包裹著作為前體或成熟形態(tài)的抗菌肽(AMPs)
和抗菌蛋白。腸道病原(帶鞭毛的紅色細(xì)菌)與腸上皮細(xì)胞的相互作用,進(jìn)入細(xì)胞,影響細(xì)胞結(jié)構(gòu)或組織,擾亂細(xì)胞功能。共生細(xì)菌(藍(lán)色和綠色細(xì)菌)主要生長(zhǎng)在腸道內(nèi)腔中粘液層外側(cè)。分泌的粘液素(黃色覆蓋在上皮表面)結(jié)合細(xì)胞膜,作為一個(gè)物理屏障保護(hù)上皮細(xì)胞表面不受到有害病原的攻擊。
隨意高度變化的指令系統(tǒng),先天性免疫系統(tǒng)使用非無(wú)性繁殖方式識(shí)別分子。腸道上皮作為宿主感應(yīng)微生物環(huán)境的一種表面,可以在需要時(shí)激活通過(guò)釋放細(xì)胞因子和趨化因子等信號(hào)分子的強(qiáng)大的防御反應(yīng),依次激活細(xì)胞的補(bǔ)充和發(fā)動(dòng)系統(tǒng)免疫細(xì)胞的攻擊。然而,不象肺部,腸道上皮容忍細(xì)菌駐留成為微生物區(qū)系的成員。盡管持續(xù)暴露給共生的細(xì)菌,正常的粘膜顯示出允許最小濃度的微生物,以回應(yīng)由駐留的革蘭氏陽(yáng)性菌和革蘭氏陰性菌引發(fā)的正常區(qū)系的大量產(chǎn)物,產(chǎn)物包括革蘭氏陰性菌產(chǎn)生的脂多糖(LPS)和革蘭氏陽(yáng)性菌產(chǎn)生的脂蛋白和肽聚糖。宿主腸道如何識(shí)別共生微生物區(qū)系和不受歡迎的腸致病性微生物的研究顯示,宿主擁有探測(cè)抗原的高度發(fā)達(dá)的系統(tǒng)。所有細(xì)菌內(nèi)源性種類(lèi)分享“自我”識(shí)別分子,稱(chēng)為微生物相關(guān)分子模式。與之相比,感染以后,作為特異性識(shí)別結(jié)果,宿主先天性粘膜免疫反應(yīng)主要被在大量病原體種類(lèi)上發(fā)現(xiàn)到的保守的“非自我”分子結(jié)構(gòu)的分子識(shí)別受體啟動(dòng),稱(chēng)為病原相關(guān)分子模式。例如,上皮細(xì)胞感應(yīng)腸內(nèi)的環(huán)境是通過(guò)他們的模式識(shí)別受體,包括TOLL樣受體 (TLRs)和核苷酸結(jié)合寡聚化結(jié)構(gòu)域(NOD)蛋白,TLR是進(jìn)化的保守蛋白,特點(diǎn)是有一個(gè)細(xì)胞外亮氨酸富集重度區(qū)域用于配體識(shí)別和細(xì)胞內(nèi)TOLL/白介素 1(IL-1)受體樣區(qū)域用于信號(hào)傳導(dǎo)。此外,在炎癥反應(yīng)中,兩種哺乳動(dòng)物的核苷酸結(jié)合亮氨酸富集重復(fù)蛋白(NOD1 和 NOD2)用作細(xì)菌產(chǎn)物的細(xì)胞內(nèi)感應(yīng)器。更特別的是,NOD2 識(shí)別一個(gè)稱(chēng)為胞壁酰二肽因子的肽聚糖片段,這種片段G- 和G+ 菌的細(xì)胞壁中都存在。
腸道上皮不僅僅是防止有害菌進(jìn)入基本組織的物理屏障,它的表面還覆蓋專(zhuān)門(mén)細(xì)胞產(chǎn)生的粘液、抗菌肽(AMPs)和抗菌分子,諸如溶解酵素,這些物質(zhì)與駐留的微生物區(qū)系共同組成抵抗致病性微生物的前線(xiàn)。本文的目的是分析我們知道的防御第一線(xiàn)。我們的分析集中在上皮中的兩種細(xì)胞系:杯狀細(xì)胞和潘氏細(xì)胞,二者在腸道防御前線(xiàn)起到關(guān)鍵作用。我們還討論最近認(rèn)識(shí)到的腸道微生物區(qū)系作為腸道病原屏障的機(jī)制。
2、粘液:
腸道粘膜表面覆蓋由特異性杯狀細(xì)胞分泌的粘液,這種杯狀細(xì)胞被稱(chēng)為粘液素分泌細(xì) 胞。
2.1、粘液素分泌細(xì)胞
粘液素分泌細(xì)胞,有一個(gè)分化的顯性特征,細(xì)胞膜頂部和底外側(cè)區(qū)域被與相鄰細(xì)胞聯(lián)系有關(guān)的 TJs 分隔開(kāi)(見(jiàn)圖 1)。在頂部區(qū)域,粘液分泌細(xì)胞有一個(gè)刷狀邊緣,一個(gè)包括有組織微絨毛的規(guī)則結(jié)構(gòu)。在腸上皮細(xì)胞,刷狀緣的微絨毛被細(xì)胞骨架組織起來(lái)的,細(xì)胞骨架包括一束肌動(dòng)蛋白細(xì)絲及與其結(jié)合的蛋白,有長(zhǎng)茸毛(Villin)和絲束蛋白。腸上皮細(xì)胞和粘液素分泌細(xì)胞的刷狀緣細(xì)胞骨架,在組織形態(tài)和維持特異性腸內(nèi)功能上起到關(guān)鍵的作用。細(xì)胞內(nèi)的微管肌動(dòng)蛋白同樣特異性組織推動(dòng)位于頂端區(qū)域邊緣空間與高爾基體之間的小泡運(yùn)
輸,這是頂端排架信號(hào)控制。在細(xì)胞核上方和刷狀緣下方,粘液素分泌細(xì)胞包含大量高電子
密度、含有被包裹著的粘液素分泌顆粒。
粘液素分泌細(xì)胞成熟從隱窩底部的增殖區(qū)開(kāi)始,他們都來(lái)源于隱窩底部的干細(xì)胞,沿著隱窩-絨毛軸遷移。粘液素分泌細(xì)胞作為分化的一個(gè)結(jié)果,與腸上皮細(xì)胞和內(nèi)分泌細(xì)胞一樣,上升到絨毛頂部、分化,接著脫落到內(nèi)腔,大約 5-7 天的短期生存時(shí)間。絨毛上的干細(xì)胞增殖和分化調(diào)控研究顯示,它們受到幾個(gè)系統(tǒng)的控制,包括Wnt和Hedgehog信號(hào)途徑、骨成形蛋白和腸轉(zhuǎn)錄因子CDX1、CDX2、HNF1。例如,標(biāo)準(zhǔn)的Wnt信號(hào)級(jí)聯(lián)包括 20 種不同的Frizzled受體交互作用。Wnt信號(hào)是通過(guò)β-catenin/TCF4 轉(zhuǎn)換,已知控制脊椎動(dòng)物多種生物現(xiàn)象,包括細(xì)胞生命期和維持特定部位干細(xì)胞、祖先細(xì)胞的預(yù)先確定的生命時(shí)間。Wnt信號(hào)在腸道上皮操縱干細(xì)胞/祖先基因程序中起到關(guān)鍵作用,祖先基因程序在腸隱窩底部附近維持未化的祖先細(xì)胞中是至關(guān)重要的。此外,最近極道,Notch信號(hào)在腸道發(fā)育中起到重要作用,因?yàn)轫敳糠置诒瓲罴?xì)胞在雙基因改造Rosa-Notch/cre+ 小鼠中激烈地衰竭。成熟的腸細(xì)胞從絨毛頂部脫落是源于被稱(chēng)為“Anoikis”的一個(gè)詳細(xì)的細(xì)胞死亡程序,這個(gè)程序受到病灶粘接素激素或β1-整合素相關(guān)元件的正向和反向控制,蛋白激素信號(hào)途徑包括磷脂酰肌醇 3 激酯/Akt、有絲分裂原活化蛋白激酶(MAPK)、應(yīng)激活化蛋白激酶(SAPK)/Jun氨基末端激酶和某些Bcl-z 與Bcl-z相關(guān)蛋白。
一系列管腔損傷被發(fā)現(xiàn)會(huì)改變杯狀細(xì)胞功能和腸粘液化學(xué)成分,管腔損傷包括正常微生物區(qū)系變化和有害腸道病原的侵?jǐn)_,但相關(guān)機(jī)制尚不清楚。研究顯示,無(wú)菌小鼠對(duì)腸致病的微生物或宿主內(nèi)源炎癥介質(zhì),粘液素基因表達(dá)、粘液成分和粘液分泌發(fā)生變化。例如,當(dāng)無(wú)菌小鼠有規(guī)律地口服從同一類(lèi)小鼠糞便中提取的微生物,細(xì)菌定植會(huì)導(dǎo)致在直腸的杯狀細(xì)胞和粘液素成分的數(shù)量上出現(xiàn)時(shí)間依賴(lài)性變化。
2.2、粘液素
請(qǐng)點(diǎn)擊鏈接下載繼續(xù)瀏覽:




